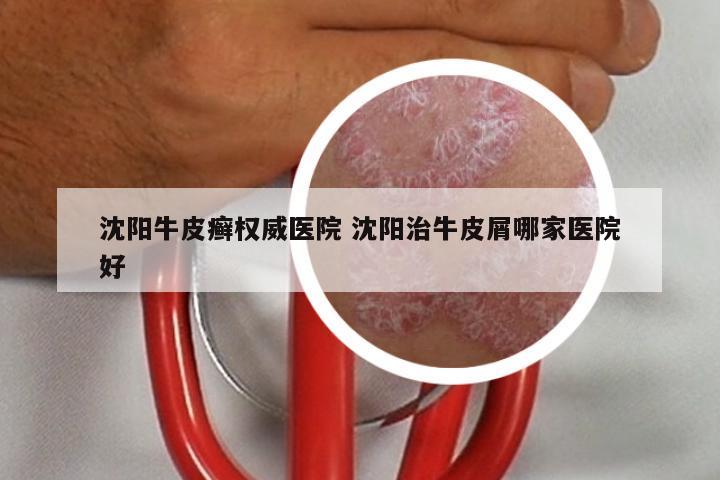
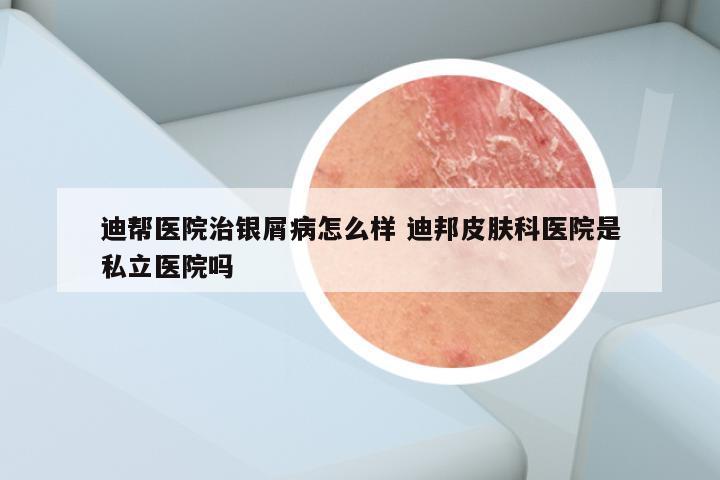
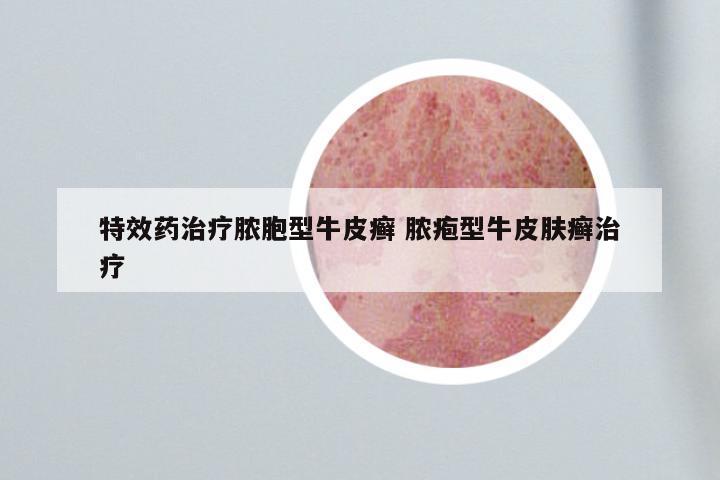
2023上市银屑病新药股票代码 生产银屑病药的上市公司
国内已上市银屑病生物制剂汇总
1、益赛普 益赛普是依那西普的国产生物制剂,于1998年11月获FDA批准上市,2006年在中国上市。适应症为银屑病治疗。单价643元,规格为25mg/支,用药方式为皮下注射,每次25mg,每周2次,每次间隔3-4天。购药优惠活动包括4赠12赠120赠28等。
2、欧泰乐(阿普米司特):作为PDE4抑制剂,用于治疗银屑病。2021年8月在中国上市,2023年纳入医保。价格:3742元/27片、942元/60片。初始剂量从第1天到第5天进行滴定,推荐维持剂量为每日口服30mg两次。
3、目前国内上市的治疗银屑病的生物制剂主要包括依那西普、英夫利昔单抗和阿达木单抗。通常通过注射用药,注入体内后,可靶向性的清除体内导致银屑病发生的炎症因子,如肿瘤坏死因子白介素-1白介素-1白介素-23等,去除相应炎症介质后,可使发病过程中的T淋巴细胞得到抑制,使皮肤病变逐渐缓解。
4、细胞因子阻断剂包括依那西普、阿达木单抗以及英利昔单抗等,而抑制T细胞和提呈细胞的生物制剂包括阿法赛特、依法利珠单抗等。此外,目前进行临床试验的还有许多生物制剂,比如巴利昔单抗等。生物制剂疗法是治疗银屑病治疗史上一大进展,但其价格昂贵,还存在不良反应等多种问题。
美国FDA批准今年第六款新药,治疗银屑病
1、美国食品药品监督管理局(FDA)近日批准了Sun Pharma公司研发的ILUMYA(tildrakizumab-asmn)用于治疗银屑病。银屑病是一种慢性免疫性疾病,特征为皮肤细胞生长周期加速,形成覆盖白色鳞屑的红色、凸起的皮肤区域,患者通常会经历瘙痒、疼痛,甚至皮肤裂开和出血。
2、截至2022年11月22日,美国FDA宣布批准uniQure与CSL Behring合作研发的AAV基因疗法Hemgenix上市,这是FDA批准的首款治疗血友病B成人患者的基因疗法,也是至今第六款上市的AAV基因疗法。
3、年9月28日,美国FDA批准“L药”用于治疗转移性皮肤鳞状细胞癌(mCSCC)或局部晚期CSCC病(laCSCC)患者,这些患者不适合接受治疗性手术或治疗性放射治疗。
4、年10月31日,美国FDA正式批准Amgen公司研发的Wezlana (ustekinumab-auub)作为Stelara (ustekinumab)的生物仿制药,用于治疗包括银屑病、银屑病关节炎、克罗恩病和溃疡性结肠炎在内的多种炎症性疾病。
5、款新药闪耀全球 2024上半年,两款核酸疗法首次获批上市,蕴含重要技术创新。Rytelo获得美国FDA批准治疗骨髓增生异常综合征,这是全球首款端粒酶靶向疗法。
新药上市|注意!新药上架了,国药专业大药房可购买
1、萨特利珠单抗,国药四川专业药房上架,为视神经脊髓炎谱系疾病(NMOSD)患者提供新选择。艾曲泊帕乙醇胺片,齐鲁制药产品,国药甘肃慢病管理专业药房。乐泰可(硫酸瑞美吉泮口崩片),国药控股云南有限公司各大药房正式开售。辉瑞口服偏头痛新药乐泰可,国药控股汉口大药房上架。
2、年10月至12月期间,国药控股专业药房在全国多个城市上架了多款新药,为患者提供了新的治疗选择。
3、不是。医生让去国药控股拿的药普遍价格昂贵,盈利性质严重,但药肯定是已经经过临床试验的经过市场考验的药品,不是新药。
4、具体时间不确定,一般在中国从新药上市申请及相关资料递送国药监的审评中心并获得受理通知书之日起算,大约在180到240个工作日完成审评事项,还需要接受新药监测期检测。关于新药注册,我国也规定了申请人在申请药品上市注册前,应当完成药学、药理毒理学和药物临床试验等相关研究工作。
3个月一针,超半数银屑病患者一年内皮肤完全清除,新药Risankizumab为啥这...
1、一项新药SKYRIZI(risankizumab)在日本取得突破,被批准用于多种银屑病类型,包括斑块性、脓疱性、红皮病性及关节炎,让全球银屑病患者瞩目。这款药物在临床试验中显示了显著优势,尤其在16周和52周的疗效上,其皮肤清除效果超过同类药物如STELARA和HUMIRA。
2、在一年内(52周), 有56%和60%的risankizumab治疗患者达到了完全皮肤清除(PASI 100), 而相对应的STELARA治疗组数据分别为21%和30%;而且在治疗斑块状银屑病3期研究没有出现新的安全事件。
3、使用PASI 100衡量,Taltz在一年期间为患者提供了大约44%的时间皮损完全清除,远超其他7种生物制剂。
4、一项一年期网络荟萃分析显示,Taltz在银屑病面积和严重程度指数(PASI)100标准下,皮损完全清除的累计益处明显优于adalimumab、brodalumab、etanercept、guselkumab、risankizumab、secukinumab和ustekinumab等药物。